Одноатомными молекулами (н. у.) образовано простое вещество:
Укажите название химического элемента:
Формулы веществ, каждое из которых состоит из атомов трех химических элементов, указаны в ряду:
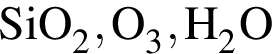
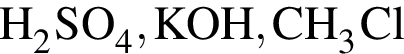
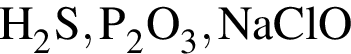

Согласно положению в периодической системе наименьший радиус имеют атомы химического элемента:
Имеются порции веществ одинакового объема (н. у.). Наибольшее число молекул содержит порция:
В кристалле 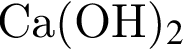 присутствуют связи:
присутствуют связи:
Укажите ряд, в котором оба гидроксида можно получить растворением соответствующего металла в воде:
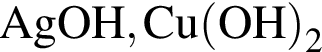
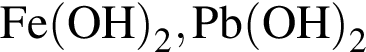
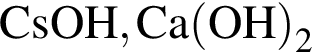
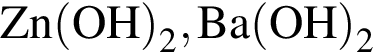
Соль образуется при взаимодействии:
Разбавленный водный раствор гидроксида калия при комнатной температуре (20 °C) может реагировать с каждым веществом пары:
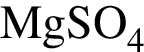
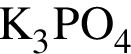 и
и 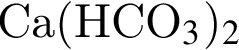 и
и Число атомов в формульной единице соли, полученной при взаимодействии избытка хлороводородной кислоты и гидроксида кальция, равно:
Укажите верное утверждение:
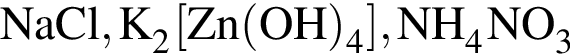 относятся к классу солей
относятся к классу солей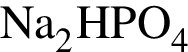 является слабым электролитом
является слабым электролитомУкажите верное утверждение относительно 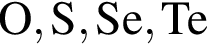 :
:
Укажите НЕПРАВИЛЬНОЕ утверждение относительно водорода:
Укажите практически осуществимые реакции (все электролиты взяты в виде разбавленных водных растворов):
а — 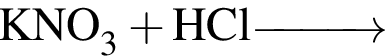
б — 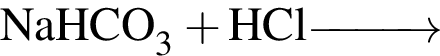
в — 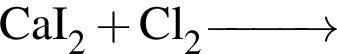
г — 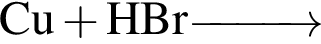
Выберите утверждения, верно характеризующие озон:
a) окислительные свойства выражены сильнее, чем у кислорода;
б) является аллотропной модификацией кислорода;
в) молекула состоит из двух атомов;
г) имеет относительную плотность по воздуху менее 1.
Исходные концентрации веществ А и В, участвующих в одностадийной реакции А + В = С, равны соответственно 2,45 моль/дм3 и 1,94 моль/дм3. Через 48 с после начала реакции концентрация вещества А снизилась до 1,37 моль/дм3. Средняя скорость (моль/дм3 · с) данной реакции и концентрация вещества В (моль/дм3) через 48 с после начала реакции равны соответственно:
Понизить жесткость воды (20 °C) можно, добавив в нее:
a — 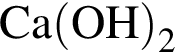
б — 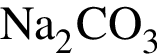
в — 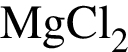
г — 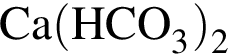
Цинковую пластинку погрузили в разбавленный водный раствор, в результате чего масса пластинки увеличилась. В исходном растворе находилось вещество:
Массовая доля металла в его оксиде ![]() равна 71,43%. Для металла справедливы утверждения:
равна 71,43%. Для металла справедливы утверждения:
а) является щёлочно-земельным металлом
б) оксид вступает в реакцию соединения с оксидом цинка при нагревании
в) получают электролизом водного раствора галогенида
г) гидроксид при нагревании разлагается на два оксида
Разбавленная серная кислота реагирует с веществами (электролиты взяты в виде водных растворов):
а — 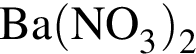
б — ![]()
в — ![]()
г — ![]()
В закрытом сосуде постоянного объёма установилось равновесие

Затем температуру повысили. Для новой равновесной системы по сравнению с первоначальной верными являются утверждения:
а) давление в системе уменьшилось
б) давление в системе увеличилось
в) израсходовался водород количеством вдвое меньшим, чем образовалась йодоводорода
г) количество йода увеличилось
Сумма коэффициентов перед веществами НЕмолекулярного строения в уравнении реакции, протекающей по схеме 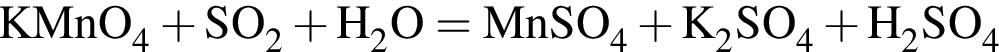 , равна:
, равна:
Укажите НЕПРАВИЛЬНЫЕ(-ОЕ) утверждения(-е):
а) присутствие фосфат-ионов в растворе можно обнаружить по реакции с нитратом серебра(I)
б) в отличие от азота фосфор НЕ взаимодействует с водородом
в) высшая валентность азота и фосфора равна IV
г) дигидрофосфат кальция может быть получен взаимодействием гидрофосфата кальция со щелочью
Окислительно-восстановительной реакцией является реакция, схема которой:
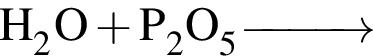
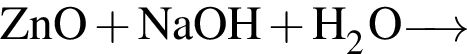
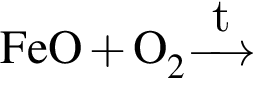
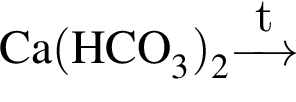
К увеличению pH водного раствора приведет:
При добавлении к воде оксида стронция:
а) рН увеличивается;
б) рН уменьшается;
в) концентрация ионов ![]() уменьшается;
уменьшается;
г) концентрация ионов ![]() НЕ изменяется.
НЕ изменяется.
Соединение, формула которого относится к классу:
Продуктом реакции присоединения является 2-метил-1,2-дихлорпентан. Исходное вещество имеет название:
Гомологи образуются при гидрировании избытком водорода углеводородов пары:
Пропин 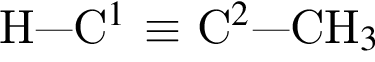 взаимодействует с избытком бромоводорода. При этом:
взаимодействует с избытком бромоводорода. При этом:
а) связь между атомами ![]() и
и ![]() укорачивается
укорачивается
б) валентный угол 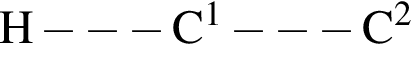 уменьшается
уменьшается
в) число ![]() -связей уменьшается
-связей уменьшается
г) протекает реакция присоединения
В результате реакции 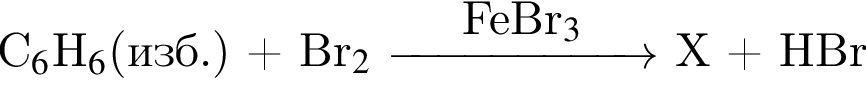
получен бромоводород количеством 0,6 моль. Масса (г) органического продукта Х составляет:
Фенол в отличие от этанола:
Для полного сжигания 0,25 моль метилбензола потребуется кислород объёмом (дм3, н. у.)
Число веществ из предложенных — 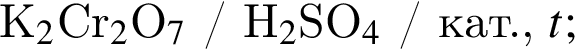
![]()
![]()
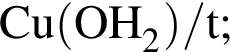
![]() которые в указанных условиях способны превратить этаналь в этановую кислоту или её соли, равно:
которые в указанных условиях способны превратить этаналь в этановую кислоту или её соли, равно:
Укажите вещество, которое в указанных условиях реагирует с этаналем:
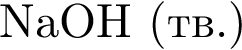
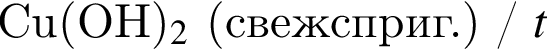
Вещества ![]() и
и ![]() в схеме превращений
в схеме превращений 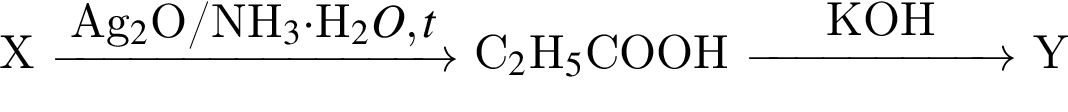 называются соответственно:
называются соответственно:
Сумма коэффициентов перед формулами продуктов в уравнении реакции полного окисления глутаминовой кислоты кислородом равна:
Мономером для получения полимера является вещество:
Газообразное (н. у.) вещество А образуется в атмосфере при грозовых разрядах. Его также получают в промышленности окислением аммиака кислородом на платиновом катализаторе. На воздухе А легко окисляется кислородом с образованием бурого газа Б, который в присутствии кислорода хорошо растворяется в воде с образованием бесцветной жидкости В. Раствор В окрашивает лакмус в красный цвет. При взаимодействии розовато-красного металла Г с концентрированным раствором В образуется газ Б и раствор вещества Д, имеющий голубую окраску. Найдите сумму молярных масс (г/моль) веществ А и Д.
Установите соответствие между названием органического соединения и общей формулой гомологического ряда, к которому данное соединение относится.
ОРГАНИЧЕСКОГО СОЕДИНЕНИЯ
А) пентаналь
Б) гексадиен-1,4
В) пропанол-2
Г) гексин-1
ГОМОЛОГИЧЕСКОГО РЯДА
1) 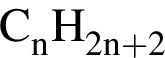
2) ![]()
3) 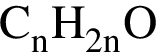
4) 
5) 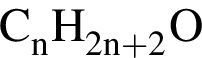
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А4Б1В5Г3. Помните, что одни данные правого столбца могут использоваться несколько раз, а другие — не использоваться вообще.
Алкин массой 82,50 г полностью сожгли в избытке кислорода. Образовавшийся углекислый газ смешали с гелием объемом (н. у.) 44,80 дм3. Молярная масса полученной при этом смеси газов составила 34,00 г /моль. Определите молярную массу (г/моль) алкина.
Определите сумму коэффициентов перед формулами продукта окисления и продукта восстановления в уравнении химической реакции, схема которой
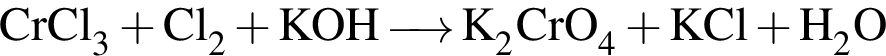
В четырех пронумерованных пробирках находятся растворы неорганических веществ. О них известно следующее:
— вещества из пробирок №1 и №4 нейтрализуют друг друга;
— вещества из пробирок №1 и №3 реагируют между собой с выделением газа (н. у.) с резким запахом, применяемого в медицине;
— при добавлении к содержимому пробирки №2 вещества из пробирки №4 выпадает белый осадок.
Установите соответствие между названием неорганического вещества и номером пробирки, в которой находится раствор данного вещества.
А) хлорид бария
Б) нитрат аммония
В) серная кислота
Г) гидроксид калия
1
2
3
4
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А1Б4B2ГЗ.
Для растворения смеси оксидов ![]() и
и ![]() массой 11 г необходимо 140 г раствора серной кислоты с массовой долей растворенного вещества 14%. Найдите массовую долю (%) кислорода в данной смеси оксидов.
массой 11 г необходимо 140 г раствора серной кислоты с массовой долей растворенного вещества 14%. Найдите массовую долю (%) кислорода в данной смеси оксидов.
В четырёх пронумерованных пробирках находятся растворы неорганических веществ. О них известно следующее:
— вещества из пробирок 1 и 4 нейтрализуют друг друга;
— вещества из пробирок 3 и 4 реагируют между собой с образованием осадка, который растворяется как в кислотах, так и в щелочах;
— при добавлении к содержимому пробирки 2 вещества из пробирки 4 образуется осадок, который на воздухе приобретает бурую окраску.
Установите соответствие между названием неорганического вещества и номером пробирки, в которой находится раствор данного вещества.
А) сульфат цинка
Б) азотная кислота
В) хлорид железа(II)
Г) гидроксид натрия
1
2
3
4
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А2Б4В3Г1.
При дегидратации насыщенного ациклического одноатомного спирта образовался алкен, объем паров которого в 12 раз меньше объема кислорода, необходимого для полного сгорания такой же порции спирта. Рассчитайте молярную массу (г/моль) спирта (объемы веществ измерены при одинаковых условиях).
Определите сумму молярных масс (г/моль) азотсодержащих веществ ![]() и
и ![]() образовавшихся в результате превращений, протекающих по схеме
образовавшихся в результате превращений, протекающих по схеме
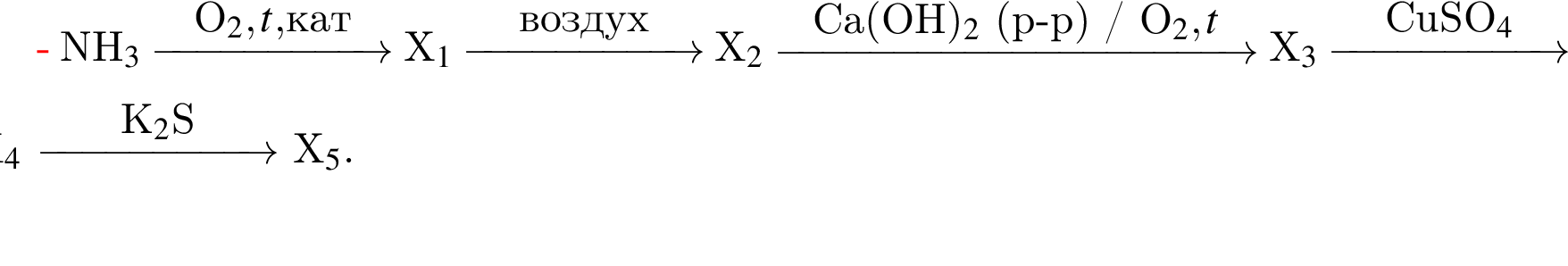
Установите соответствие между схемой химической реакции, протекающей в водном растворе, и суммой коэффициентов в сокращенном ионном уравнении реакции.
А) 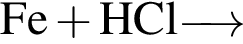
Б) 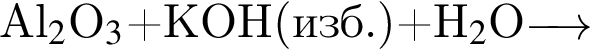
В) 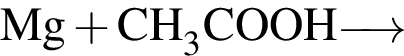
Г) 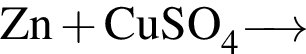
1) 3
2) 4
3) 5
4) 6
5) 7
6) 12
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А2Б3В5Г1.
Расставьте коэффициенты методом электронного баланса в уравнении окислительно-восстановительной реакции, схема которой
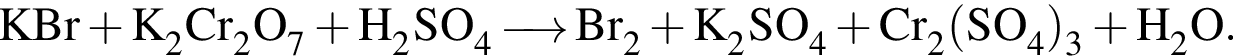
Укажите сумму коэффициентов перед веществами молекулярного строения.
К 30 дм3 смеси, состоящей из пропана и аммиака, добавили 10 дм3 хлороводорода. После приведения новой газовой смеси к первоначальным условиям ее относительная плотность по воздуху составила 0,80. Укажите массовую долю (%) пропана в исходной смеси. (Все объемы измеряли при t = 20 °C, Р = 105 Па.)

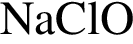 подходит под условие задачи. В ряду
подходит под условие задачи. В ряду 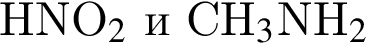 . А вот
. А вот 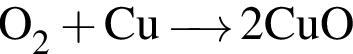

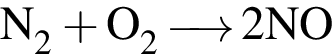
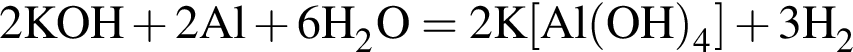
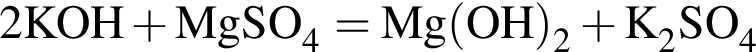

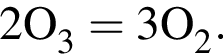
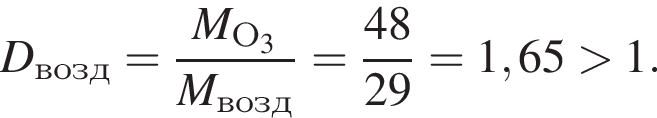
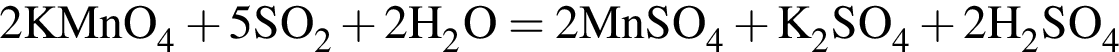
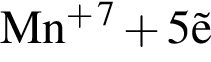 →
→ 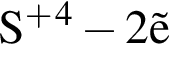 →
→ 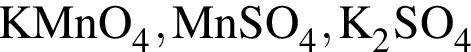 - вещества ионного строения,
- вещества ионного строения,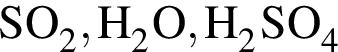 - вещества молекулярного строения.
- вещества молекулярного строения.
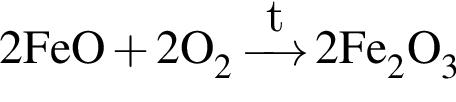
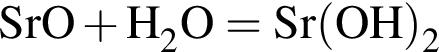
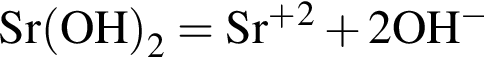
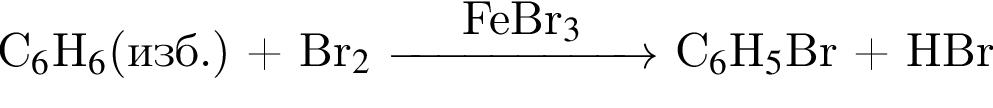
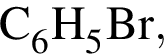 учитывая стехиометрические коэффициенты уравнения реакции, очевидно, что:
учитывая стехиометрические коэффициенты уравнения реакции, очевидно, что:
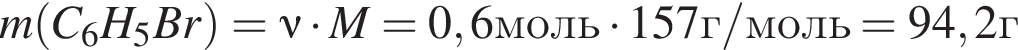
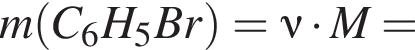
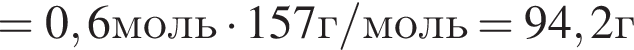
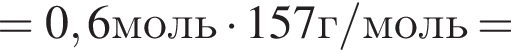
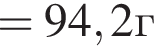

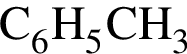 ) =0,25 моль (по условию задачи)
) =0,25 моль (по условию задачи)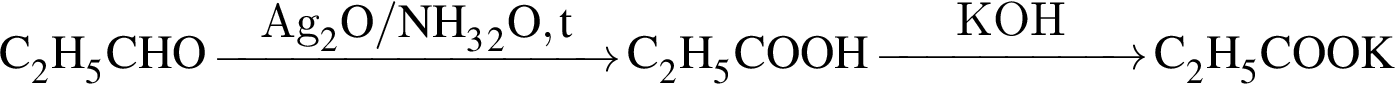
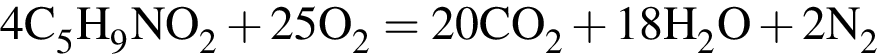
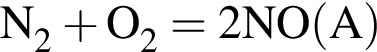
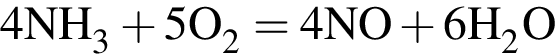
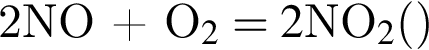
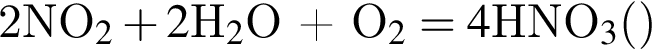
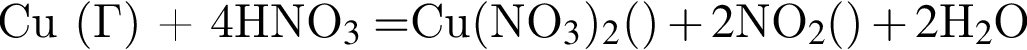
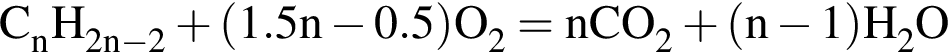
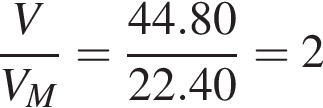
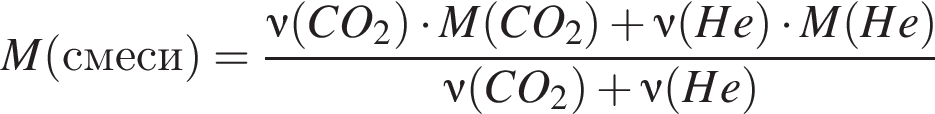
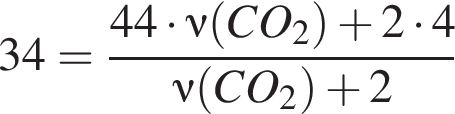
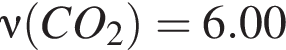 моль
моль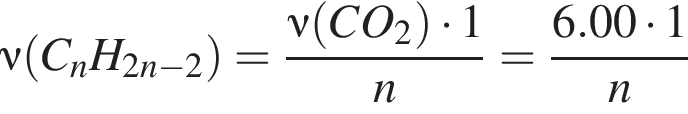
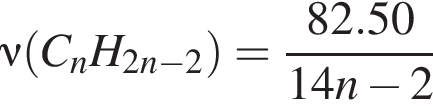
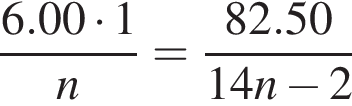
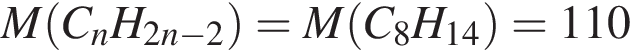 г/моль
г/моль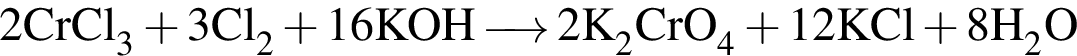



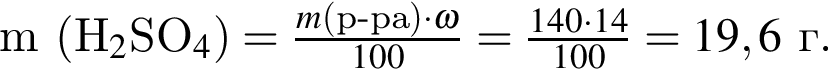
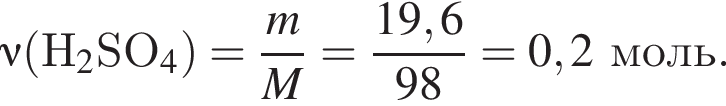
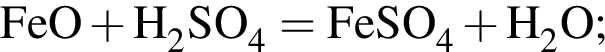
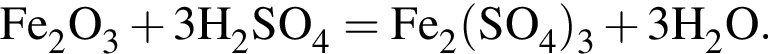
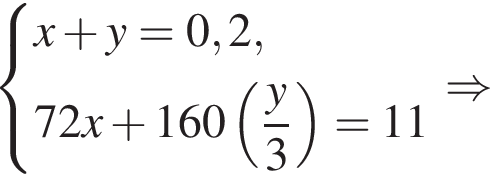
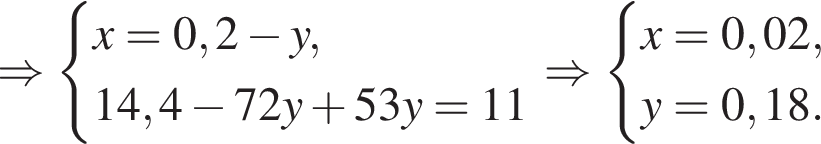
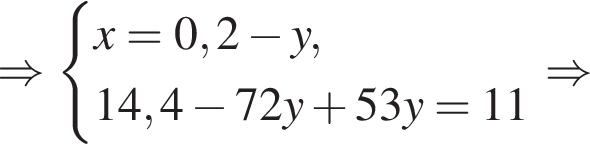
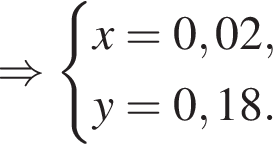
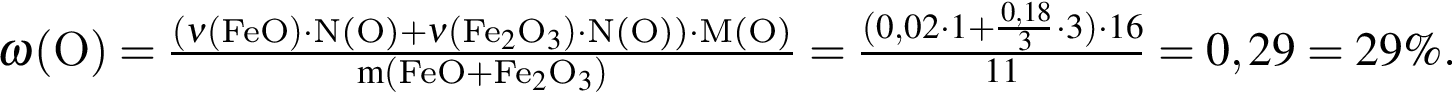
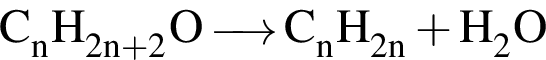
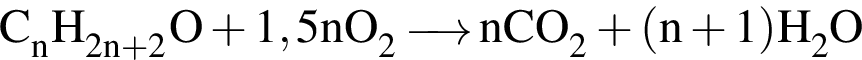
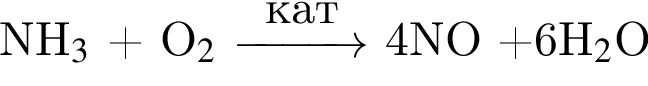
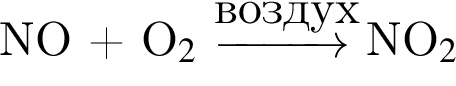
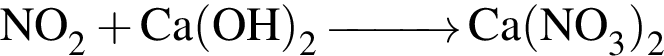

 ↓
↓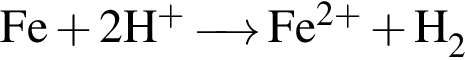 . Сумма коэффициентов — 5.
. Сумма коэффициентов — 5.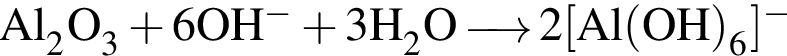 . Сумма коэффициентов — 12.
. Сумма коэффициентов — 12.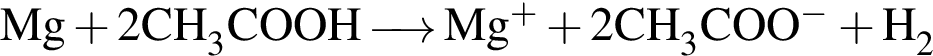 . Сумма коэффициентов − 7.
. Сумма коэффициентов − 7.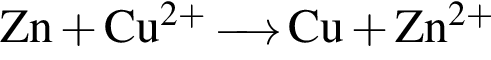 . Сумма коэффициентов − 4.
. Сумма коэффициентов − 4.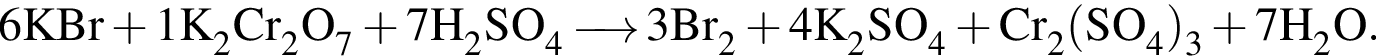
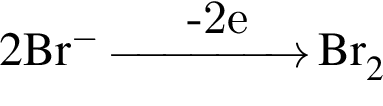
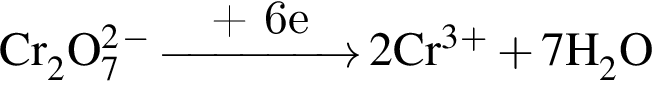
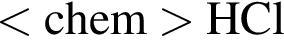
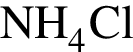
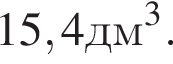 Следовательно, в исходной смеси объем аммиака = 15,4+10 = 25,4
Следовательно, в исходной смеси объем аммиака = 15,4+10 = 25,4